Construction of chlorogenic acid-containing liposomes with prolonged antitumor immunity based on T cell regulation
这篇论文研究了绿原酸(CHA)作为潜在的癌症免疫治疗剂,特别是通过制备含有CHA-磷脂复合物(PC)的聚乙二醇化脂质体(CHA-PC PEG-Lipo,简称CPPL)来降低给药频率。
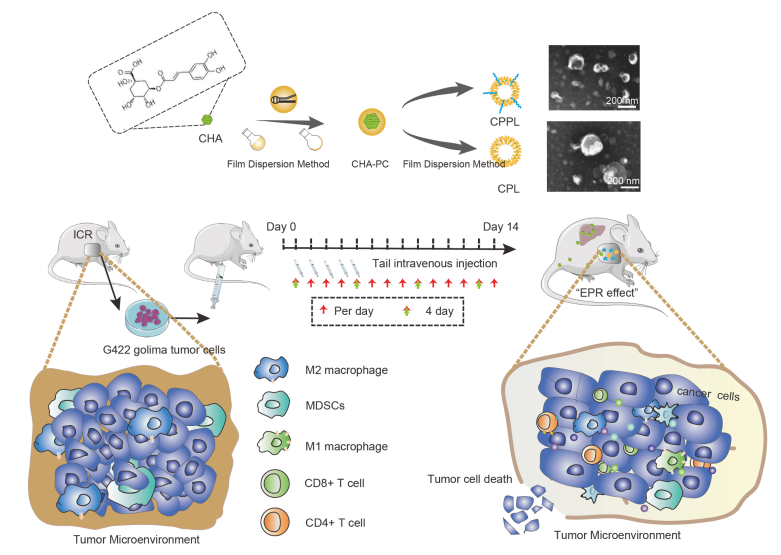
CHA-PC脂质体的制备和给药方案
研究背景
1、癌症是全球主要致死疾病之一,传统化疗效果有限且副作用显著,尤其在肿瘤转移和复发时效果不佳。
2、免疫治疗虽然显示出潜力,但药物耐药性削弱了其效果。此外,天然药物如绿原酸(CHA)虽然具有多种药理效应,但其体内不稳定性和低口服生物利用度限制了临床应用。
3、现有研究表明,CHA具有抗氧化、抗菌、抗炎、抗肿瘤和免疫调节等多种生物活性,但其低口服生物利用度和短半衰期需要频繁注射,导致患者依从性差。
研究方法
1、制备了CHA-PC,并将其包封在脂质体和PEG化脂质体中,分别命名为CPL和CPPL。
2、通过动态光散射(DLS)和透射电子显微镜(TEM)对CPL和CPPL的形态、粒径、多分散指数(PDI)、zeta电位和包封效率进行了表征。
4、在4°C下评估了CPL和CPPL的储存稳定性,并在模拟体内环境的培养基中评估了其体外稳定性。
5、通过高效液相色谱(HPLC)和液相色谱-质谱联用(HPLC-MS/MS)分析了CPL和CPPL在大鼠体内的药代动力学和体内分布。
6、使用G422小鼠胶质瘤细胞异种移植模型评估了CPL和CPPL的抗肿瘤效果,并通过流式细胞术和免疫组化分析了其对免疫细胞的影响。
实验设计
1、CPL和CPPL的粒径分别为220.37±0.75 nm和149.73±0.50 nm,包封效率均约为60%。
2、在4°C下储存30天后,CPL和CPPL的粒径、PDI、zeta电位和包封效率均无明显变化,表明其具有良好的储存稳定性。
3、在模拟体内环境的培养基中,CPPL的稳定性优于CPL,表明其在体内环境中更稳定。
4、药代动力学研究表明,CPPL显著延长了CHA在体内的循环时间,并增加了其在肿瘤中的积累。
5、在抗肿瘤效果评估中,CPPL在延长给药间隔至4天的情况下仍能保持与每日给药相同的抗肿瘤效果,而CHA溶液和CPL在延长给药间隔后抗肿瘤效果显著下降。
结果与分析
1、CPPL通过刺激CD4+和CD8+ T细胞浸润、抑制髓源性抑制细胞(MDSCs)表达、减少2、Th2相关因子的表达以及增加肿瘤组织中的记忆T细胞,表现出优异的抗肿瘤免疫效果。
3、CPPL显著增加了肿瘤组织中的记忆T细胞(TEM和TCM),并提高了其在淋巴结中的比例,促进了长期免疫记忆的形成。
4、CPPL在延长给药间隔至4天的情况下仍能保持与每日给药相同的抗肿瘤效果,而CHA溶液和CPL在延长给药间隔后抗肿瘤效果显著下降。
总体结论
1、通过使用PEG化脂质体包封CHA,显著提高了CHA的体内稳定性和抗肿瘤免疫效果。
2、CPPL在延长给药间隔的情况下仍能保持优异的抗肿瘤效果,表明其在癌症治疗中具有重要的临床应用潜力。
这篇论文展示了CHA-PC PEG-Lipo在癌症免疫治疗中的潜力,特别是在延长给药间隔方面的优势。


