Science子刊:陈亮|刘宝辉|顾颖揭秘胶质母细胞瘤的“变形术”与复发之谜
胶质母细胞瘤(GBM)是脑肿瘤中的“绝症”。它为何如此可怕?即便手术、放疗、化疗“三板斧”齐上阵,患者的中位生存期也只有15个月。这种肿瘤就像一场永无止境的“攻防战”,即使“铲除”了看得见的肿瘤,依然会有隐藏的细胞伺机卷土重来,促成复发。
究其原因,GBM的两大特性至关重要:异质性和侵袭性。
·“千人千面”的肿瘤细胞
GBM的异质性体现在,它的肿瘤细胞不是一个模子刻出来的,而是呈现出四种主要状态:NPC-like(神经前体样),OPC-like(少突胶质细胞前体样),AC-like(星形胶质细胞样),MES-like(间充质样)。这些状态可以互相转变,就像变形金刚一样,随时适应环境变化。更令人头疼的是,这种“变形术”帮助肿瘤细胞在治疗压力下迅速产生耐药性,躲避清除。
·“潜伏者”的扩散术
另一大难点是GBM的侵袭性。肿瘤细胞会悄悄渗透到正常脑组织中,化身“潜伏者”,在远离肿瘤核心区域的地方伺机潜伏。一旦治疗结束,这些隐匿的细胞便会重新活跃,引发复发。
新发现:肿瘤细胞的区域特性
2024年11月22日,华大研究院陈亮、顾颖团队和武汉大学刘宝辉团队在Science Advances上发表了题为Single-cell multi-omics sequencing uncovers region-specific plasticity of glioblastoma for complementary therapeutic targeting的研究。在此研究中,科学家使用华大平台的单细胞核RNA测序(snRNA-seq)和单细胞核染色质开放测序(snATAC-seq)技术,对GBM患者的样本进行了系统分析。这些技术帮助科学家不仅观察到肿瘤细胞的基因表达,还可以捕捉到其表观遗传特征,为揭示肿瘤的区域特性提供了全新视角。研究人员已将数据上传至CNGB网站(https://db.cngb.org/cnsa/; CNP0003766),并构建了在线版网页,方便研究人员探索(https://db.cngb.org/cdcp/visualization?project=CNP0003766)。
·结果1:状态转变的特征
研究发现,肿瘤核心区(TC)的肿瘤细胞更倾向于呈现星形胶质细胞样(AC-like)状态,而在肿瘤周围脑组织区(PTB),少突胶质细胞前体样(OPC-like)细胞占据主导地位。这种变化可能意味着:1)肿瘤细胞通过环境适应实现转变。在侵袭周围组织时,肿瘤细胞可能通过与局部健康细胞的相互作用,获取神经前体的特征。2)某些状态细胞更具扩散性。研究也指出,具有较高OPC-like状态的肿瘤细胞可能更容易扩散至周围组织。
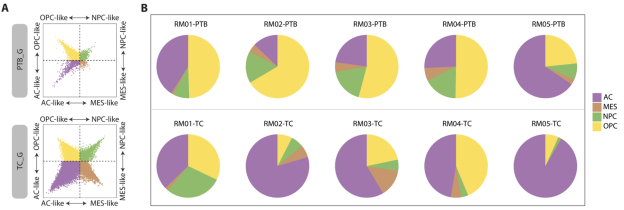
图1 肿瘤细胞在PTB区状态发生改变
·结果2:关键转录因子的调控差异
进一步分析揭示,肿瘤核心区域和周围区域的细胞在分子调控上也存在显著差异。激活蛋白1(AP-1)在肿瘤核心区活性较高,但在周围区域逐渐减弱。BACH1在周围区域的活性显著增强。这两种转录因子在肿瘤的侵袭性和状态转变中扮演着重要角色。研究表明,仅抑制AP-1可能不足以彻底清除扩散的肿瘤细胞,而BACH1的活性提升为治疗提供了新的潜在靶点。
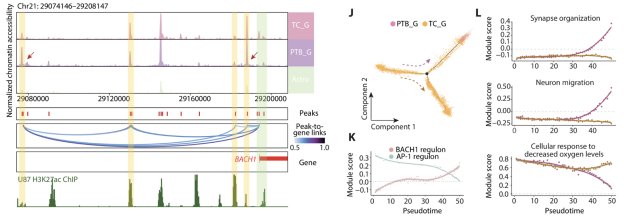
图2 肿瘤细胞在侵袭后转录调控发生变化
·结果3:联合治疗的潜力
为了验证这些转录因子在GBM治疗中的潜力,研究团队设计了一系列功能实验,探索联合靶向AP-1和BACH1的治疗效果。这一策略在小鼠模型中表现出了显著的疗效。
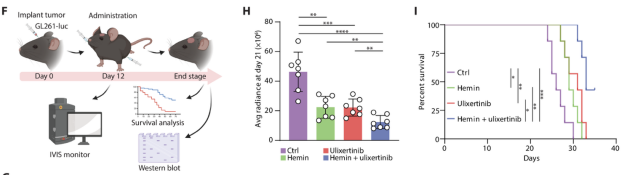
图3 联合治疗显著提高疗效
新方向:区域特性治疗
这项研究为GBM的治疗提出了全新思路。通过深入剖析肿瘤细胞的区域异质性,研究不仅揭示了肿瘤的分子调控机制,还为未来的双靶点联合治疗提供了坚实的理论基础。
如果GBM是一场攻防战,那么了解“变形术”和“潜伏术”就是破解其复发难题的关键。而这种基于区域特性的精准治疗策略,或将为癌症研究开启新的篇章。
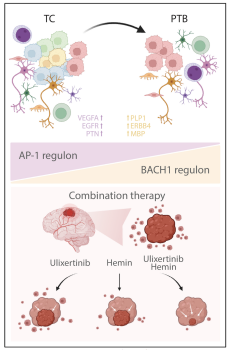
图4 靶向胶质母细胞瘤异质性与浸润性的治疗新方案
参考消息:
https://www.science.org/doi/10.1126/sciadv.adn4306

内容为【iNature】公众号原创,来源于【iNature】
声明:本文仅用于分享,不代表平台立场,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!


